Vse o osmiju

Osmij - redka kovina, spada v skupino platine. Odkrili so ga v Angliji kot rezultat poskusov reakcije platine. Ime osmij je podano v grščini in v prevodu pomeni "vonj". Kaj je ta plemenita kovina? Kakšne so njegove značilnosti in kakšne so njegove prednosti?

Zgodba
Ta element sta po naključju leta 1803 odkrila angleška kemika Smithson Tennant in William H. Wollastan. Kot rezultat poskusov reakcije platine na mešanico kislin (žveplove in dušikove) se je v nastali oborini pojavil neprijeten vonj, ki je spominjal na smrad klora in gnile redkve. Podobne poskuse so izvedli Collet-Descoti, Antoine de Fourquoy in Vauquelin v Franciji. Kot rezultat svojih raziskav so našli tudi njim neznano snov v netopni oborini iz platine.



Takrat neznana snov je dobila ime Pten, vendar so poskusi Britancev dokazali, da gre za dve podobni snovi - iridij in osmij.
Tennantovo pisno sporočilo z dne 21. junija 1804 je londonski kraljevi družbi predstavilo odkritje teh kemičnih elementov. V periodnem sistemu kemičnih elementov Mendelejeva se kovina nahaja pod zaporedno številko 76. V svoji čisti obliki kovine ni v zrncih, zato je njena kemijska formula predstavljena v raztopljeni obliki.


Pridobivanje elementa poteka iz sekundarnih surovin kot posledica njegove ločitve od iridijeve, platinske, platinasto-paladijeve rude ali bakrove in nikljeve rude. Letna proizvodnja celotnega elementa na svetu ne presega velikosti 1 tone.


Kraj rojstva
Največja nahajališča na svetu so vredna pozornosti na takih območjih, kot so Uralske gore in Sibirija v Rusiji, severna država Aljaska in zahodna država Kalifornija v Ameriki, Kanada v Severni Ameriki, Kolumbija v Južni Ameriki in nekaj Južnoafriške države, Avstralija, otok Tasmanija. Trenutno se šteje veliko nahajališče osmija Kompleks Bushwell v Južni Afriki, kjer se koplje večina snovi. Glede na to, da so največja nahajališča kovine v Južni Afriki, so svetovne cene te redke zemeljske kovine precej visoke. Kazahstan velja za edinega velikega izvoznika osmija-187 na svetu. Čeprav ima Kitajska zaloge platinske rude, nima pomembne količine osmija.


Snov je shranjena v prahu in ker se ne topi v obliki kristalov, je zaradi njenih fizikalnih lastnosti ni mogoče označiti. Za izdelavo ingotov te kovine se uporablja ogrevanje z elektronskim žarkom ali oblokom iz prahu, uporablja pa se tudi ogrevanje v lončku.


Lastnosti
Osmij je videti kot modrikasto srebrna kovina. To je eden najgostejših elementov, njegova gostota je 22.600 kilogramov na kubični meter, hkrati pa je snov precej krhka, zlahka se zlomi in drobi.Ima visoko specifično težo in lahko sveti tudi pri dokaj visokih temperaturnih učinkih. Zaradi parametrov in znatne temperature taljenja ga je težko strojno obdelati. V naravi obstaja v obliki sedmih izotopov, od katerih jih šest velja za stabilne, to so osmij-184, osmij-187, osmij-188, osmij-189, osmij-190 in osmij-192. Radioaktivne kovinske izotope z masnimi števili od 162 do 197 so pridobili v laboratoriju, nekatere jedrske izomere pa tudi umetno.
Osmij po svojih lastnostih negativno vpliva na vse žive organizme.

Skoraj vse spojine s to kovino povzročajo poškodbe notranjih organov, motnje vida in sluha. V primeru zastrupitve z osmijevimi hlapi lahko pride do nepopravljivih poškodb telesa in smrti. Znanstveniki so izvedli poskuse na živalih, katerih rezultati so bili hiter razvoj anemije, pomanjkanje normalnega delovanja pljučne funkcije. Ugotovljeno je bilo, da gre za hitro razvijajoč se edem. Osmijev tetroksid, ki se uporablja v medicini, je zelo agresivna snov. Ima najbolj odvraten vonj na svetu. V primeru zastrupitve koža trpi, spremeni barvo v zeleno ali črno, pogosto to spremljajo razjede in razpoke, ki se celijo zelo dolgo.

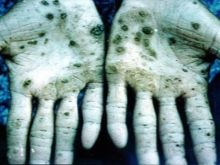

Najbolj ogroženi so zaposleni v industrijskih prostorih, ki v skladu z vsemi varnostnimi standardi delajo samo v respiratorjih in posebnih oblačilih. Vse posode, ki vsebujejo osmijev oksid, so zaprte in skladiščene v skladu s predpisi. Za pridobivanje nevyanskitnih mineralov se platina pretvori v raztopino z uporabo aqua regia. Nato nastalo oborino obdelamo z 8-kratnim cinkom - taka zlitina relativno enostavno preide v praškasto stanje, ki se nato stopi z barijevim peroksidom. Naslednji korak je obdelava nastale mase s pomočjo vodke, destilacija skozi aparat za ločevanje osmijevega tetroksida.

Z izpostavitvijo snovi raztopini alkalije dobimo sol. Raztopina soli je prizadeta hiposulfit, zaradi česar se kovina s pomočjo amonijevega klorida izloči že v obliki Fremyjeve soli. Oborino speremo, filtriramo in kalciniramo. Rezultat vseh teh dejanj je gobast osmij. Nato ga očistimo s kislinami, reduciramo v električni peči pod tokom vodika in ohladimo. torej pridobite vzorce osmija do 99,9 %.


Kemični
Lastnosti tega elementa so s kemijskega vidika neverjetne. Najpomembnejši med njimi so naslednji.
- Osmij sploh ne reagira z alkalijami in kislinami. V reakciji z alkalnimi talinami tvori vodotopne osmate. Interakcija z mešanico dušikove in klorovodikove kisline povzroči izjemno počasno reakcijo.
- Zelo strupeno, tudi v mikroskopskih odmerkih. Posebej strupen je osmijev oksid, ki je izoliran iz platine.
- Vrelišče kovine ni mogoče določiti, ker je še posebej ognjevzdržna.
- Kovina v prahu zlahka vstopi v reakcijo segrevanja s takšnimi snovmi: čisti kisik, halogeni, žveplova ali dušikova kislina.
- V različnih spojinah dobi oksidna števila od -2 do +8. Najpogostejši so +2, +3, +4 in +8.
- Sposoben tvorjenja grozdnih spojin.
- Glavni minerali so povezani s trdnimi raztopinami in jih predstavljajo zlitine iridija z osmijem - to sta sysertskit in nevyanskit. Poleg tega ima Syserskite drugačno ime - osmijev iridij in nevjanskit - osmijev iridij.

Fizično
Gostota osmija je približno 22,61 grama na kubični centimeter. Kristali imajo čudovit srebrn lesk, z različnimi odtenki od sive do modre. V ingotovih se pojavi temno modra barva, v prahu - vijolična. Vse kovine imajo srebrn lesk. Toksičnost elementa ne dovoljuje njegove uporabe v industriji nakita. Glavne fizikalne lastnosti so navedene na naslednji način.
- Tališče tega elementa je precej visoko, taljenje je možno pri temperaturah nad 3000 stopinj Celzija.
- Kovina nima magnetnih lastnosti.
- Neverjetna trdota. Zlitine z dodatkom te kovine pridobijo povečano odpornost proti obrabi, vzdržljivost, odpornost proti koroziji, odpornost na mehanske obremenitve.
- Vrelišče je 5012 ºC.
- Mohsova trdota je 7.
- Vickersova trdota je 3-4 GPa.

Aplikacije
Zaradi znatnih stroškov samega elementa se ta kovina redko uporablja v masovni industrijski proizvodnji. V osnovi področje uporabe osmija predstavlja industrija v kemični industriji, kjer se uporablja kot katalizator. Osmijev tetroksid se uporablja v nekaterih zdravilih. V laboratorijskih preiskavah se uporablja za barvanje živih tkiv, zagotavlja ohranjanje strukture celic.
V vesoljski industriji se uporablja osmij v elektronski opremi opreme za letalsko in raketno tehniko, kot tudi pri izdelavi jedrska orožja. Zaradi pomanjkanja magnetnih lastnosti, kovina se uporablja pri izdelavi ročnih ur, kot je Rolex. Uporablja se zlitina osmija in platine izdelava kirurških vsadkov To so srčni spodbujevalniki ali pljučne zaklopke.
Poleg tega se osmij uporablja v mikroskopiji in za izdelavo visoko natančnih instrumentov.



Zanimiva dejstva
- Pod tlakom približno 770 GPa v osmiju elektroni medsebojno delujejo v notranjih orbitalah, struktura snovi ostane nespremenjena.
- Osmij kamnine vsebujejo pol odstotka celotne mase rudnih nahajališč.
- Zaradi visoke gostote videz in dejanska masa kovine se zelo razlikujeta. Tako bo 0,5-litrska plastična steklenica, napolnjena s tem kovinskim prahom, težja od 10-litrskega vedra, napolnjenega z vodo.
- Ta kovina je med prvih pet drago.
- Cena trojne unče osmija je poslovna skrivnost, v odprtih virih lahko najdete približno ceno za 1 gram snovi.
- Zaradi ognjevzdržnosti osmija zabeležen v zgodovini električne svetilke. Znanstvenik K. Auer von Welsbach iz Nemčije je predlagal zamenjavo ogljikove nitke v žarnici z osmijevo. Izkazalo se je, da so žarnice 3-krat manj energetsko intenzivne, osvetlitev pa se je opazno izboljšala. Res je, da ga je kmalu nadomestil pogostejši tantal, ki pa ga je nadomestil volfram.
- Podobna situacija se je zgodila z redko kovino pri proizvodnji amoniaka. Trenutno uporabljena metoda za sintezo amoniaka, ki jo je leta 1908 razvil kemik Fritz Haber iz Nemčije, je nemogoča brez uporabe katalizatorjev.Sprva so takrat uporabljeni katalizatorji pokazali svoje lastnosti le v prisotnosti pomembnih temperaturnih pogojev in niso imeli visoke učinkovitosti, zato je bilo iskanje zamenjave zelo pomembno. Znanstveniki iz laboratorija Visoke tehnične šole v Karlsruheju so predlagali uporabo fino dispergiranega osmija kot katalitičnega elementa. Rezultati testiranja so potrdili, da je bila ideja vredna truda, katalitska temperatura se je znižala za več kot 100 ºC, proizvodnja amoniaka pa se je znatno povečala. Res je, da je bil osmij v prihodnosti opuščen, vendar je pomagal pri reševanju tako pomembnega problema.

Osmij in druge redke in edinstvene kovine igrajo pomembno vlogo v različnih panogah. Kljub vsej svoji toksičnosti rešuje življenja in zdravje ljudi.
Več informacij o osmiju lahko dobite v naslednjem videu.








